|
Разные: Новый антибиотик обманывает устойчивые к лекарствам бактерии с помощью мимикрии
|
Большинству антибиотиков необходимо проникнуть в бактерии для их уничтожения. Даробактин, недавно открытое соединение, слишком велик для этого. Тем не менее, он убивает множество устойчивых к антибиотикам патогенов, используя крошечное слабое место на их поверхности. Исследователи из Швейцарии использовали этот механизм для создания мимикрирующих антибиотиков.
Все большее количество бактериальных патогенов устойчивы к антибиотикам. У самых опасных из них есть общая особенность: двойная мембрана, через которую трудно проникнуть. Даже когда антибиотикам удается это, бактерии просто «выбрасывают» их обратно. Но недавно обнаруженному соединению под названием даробактин (darobactin) удается обойти эти защитные меры и убить почти все проблемные патогены. Он представляет собой короткий пептид, состоящий из семи аминокислот, синтезирующийся на рибосомах, как обычные клеточные белки.
Теперь исследователи смогли выяснить механизм его действия. Его форма имитирует особую трехмерную структуру. Обычно ее находят только в белках, производимых бактериями в качестве строительных блоков для их внешней мембраны. Структура является «ключом» для вставки белков во внешнюю оболочку в определенных местах. Даробактин — копия этого ключа. Однако он не может проникнуть в бактерии, а просто блокирует «замочную скважину» снаружи. В результате затрудняется транспорт компонентов оболочки бактерий, и они погибают.
Подобные механизмы уже известны в микробиологии и используются другими лекарствами. Однако даробактин больше, чем большинство лекарств, и не может проникнуть через входные порты бактерий.
Оказалось, что у бактерий за формирование внешней мембраны отвечает мутация в гене белка BamA. Даробактин атакует «ахиллесову пяту» патогенов. Он напрямую связывается с наиболее важным участком белка, так называемыми атомами основной цепи. Поскольку эти атомы удерживают белок вместе и определяют его форму, их почти невозможно изменить (изменение как раз является обычным для бактерий способом отразить новый антибиотик. Фактически даробактин сохранил свою эффективность против всех патогенов, для которых Хиллер и его команда провели лабораторные испытания, имитирующие устойчивость. Другими словами, патогенам не удалось изменить «сломанный замок».
Ученые нашли психоделики без галлюциногенного эффекта для лечения депрессии
Ученые из Калифорнийского университета определили психоделик, который может ускорить процесс лечения психических расстройств, включая депрессию, не вызывая при этом галлюцинаций. Об этом сообщает The Guardian.
Согласно исследованию, особый интерес ученых вызвало ранее не изученное негаллюциногенное соединение AAZ-A-154. Его свойства проверили в исследованиях на животных, и оно оказало влияние, аналогичное влиянию классических галлюциногенных психоделиков.
«Препарат в настоящее время проходит испытания на безопасность, перед тем,как попасть на ранние стадии испытаний на людях», — заявил Дэвид Олсон (David Olson), доцент кафедры химии Калифорнийского университета.
Психоделик — это лекарственный препарат на основе наркотического вещества, изменяющего сознание. Исследователи стремятся использовать терапевтический потенциал психоделиков для лечения депрессии и посттравматического расстройства. В то время как нейролептики обычно работают, изменяя химический состав мозга, психоделики способствуют пластичности нейронов, по сути позволяя мозгу перестраиваться.
Издание указывает, что ученые из лондонского Имперского колледжа ранее обнаружили эффективность «волшебных грибов», содержащих псилоцибин, при лечении среднего и тяжелого депрессивного расстройства.
Ранее диетологи назвали продукты для борьбы с депрессией. Среди повышающих настроение продуктов специалисты назвали темный шоколад, жирную рыбу и яичные желтки.

Фото: Jason Langley / imageBROKER.com / Globallookpress.com
Яд паука остановит гибель нервных клеток
Международная группа ученых, в состав которой входят сотрудники МФТИ, наглядно показала, что яд паука-кругопряда Argiope lobata можно использовать для блокировки активности нейрорецепторов мозга человека.
Полученные результаты позволят создать препараты для лечения многих нейродегенеративных заболеваний. Исследование опубликовано в журнале Neuron.
Быстрая передача сигнала между нейронами нашего мозга в подавляющем большинстве случаев происходит за счет выброса передающим нейроном специального сигнального соединения — нейромедиатора, который воздействует на принимающий нейрон. В зависимости от эффекта, нейромедиаторы подразделяют на возбуждающие и тормозные. Нейромедиатор глутамат в головном мозге человека активирует нейроны за счет присоединения к специальным белкам, встроенным в мембрану, — глутаматным рецепторам — и открытия в них ионного канала, пропускающего положительно заряженные ионы.
Открытие каналов глутаматных рецепторов приводит к деполяризации мембраны и возникновению потенциала действия, который затем распространяется по отросткам нейрона. При заболеваниях нервной системы происходит излишняя активация глутаматных рецепторов, в особенности тех, которые хорошо проводят кальций. Попадание в принимающие нейроны слишком большого количества кальция запускает процессы апоптоза и приводит к гибели нервных клеток. Поэтому стоит задача разработки специальных блокаторов для регулирования этого процесса.
Исследователям удалось изучить молекулярную структуру комплекса глутаматного рецептора с тремя блокаторами, включая природный токсин аргиопин из яда паука-кругопряда Argiope lobata и два искусственных соединения. Химическая формула всех трех блокаторов состоит из двух частей: «головы», напоминающей остаток ароматической аминокислоты, и «хвоста» различной длины, включающего аминогруппы, соединенные алифатическими углеводородными линкерами. Наблюдения производились с помощью метода криоэлектронной микроскопии, за развитие которого в 2017 году была присуждена Нобелевская премия Жаку Дюбоше, Иоахиму Франку и Ричарду Хендерсону.
 Рисунок 1: Химические формулы блокаторов глутаматных рецепторов, использованных в работе / Пресс-служба МФТИ
Рисунок 1: Химические формулы блокаторов глутаматных рецепторов, использованных в работе / Пресс-служба МФТИ
«Оказалось, что эти блокаторы проникают внутрь рецептора, когда тот открывается при действии глутамата, при этом они помещают свой положительно заряженный хвост в узкую отрицательно заряженную часть ионного канала — его селективный фильтр, обусловливающий способность пропускать только катионы. Пройти канал насквозь блокаторам не позволяет их голова, застревающая во внутренней полости рецептора», — объясняет руководитель работы Александр Соболевский, выпускник МФТИ и заведующий лабораторией в Колумбийском университете (Нью-Йорк, США).
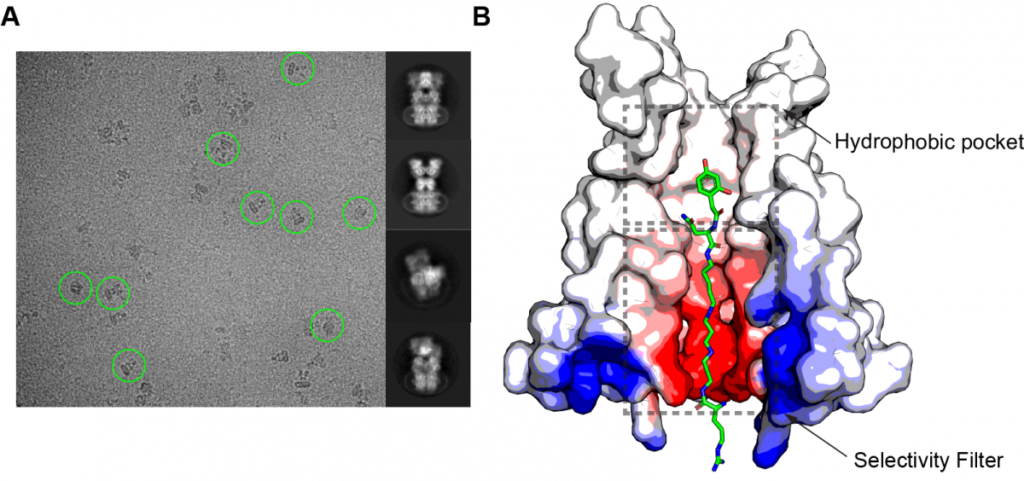 Рисунок 2: Структура комплекса глутаматного рецептора и токсина паука Argiope lobata — ацилполиамина аргиопина. (A) Микрографическая картинка, полученная с помощью криоэлектронной микроскопии, где изображения нескольких молекулярных комплексов обведены для примера зелеными кругами (слева), и примеры усредненных изображений молекулярных комплексов (справа). (B) Структура поры ионного канала рецептора с молекулой аргиопина внутри. а / Пресс-служба МФТИ, рисунок предоставлен Эдвардом Твуми, бывшим студентом лаборатории А. Соболевского, ныне сотрудником Гарвардского университета
Рисунок 2: Структура комплекса глутаматного рецептора и токсина паука Argiope lobata — ацилполиамина аргиопина. (A) Микрографическая картинка, полученная с помощью криоэлектронной микроскопии, где изображения нескольких молекулярных комплексов обведены для примера зелеными кругами (слева), и примеры усредненных изображений молекулярных комплексов (справа). (B) Структура поры ионного канала рецептора с молекулой аргиопина внутри. а / Пресс-служба МФТИ, рисунок предоставлен Эдвардом Твуми, бывшим студентом лаборатории А. Соболевского, ныне сотрудником Гарвардского университета
«Полученная информация может быть использована для создания селективных блокаторов глутаматных рецепторов, пропускающих ионы кальция и являющихся важной фармакологической мишенью в целом ряде заболеваний, включая боковой амиотрофический склероз (болезнь Шарко), эпилепсию, гибель нейронов при ишемии и нейродегенерацию при болезнях Альцгеймера и Паркинсона», — рассказывает Мария Елшанская, выпускник МФТИ и научный сотрудник Колумбийского университета.
«Примечательно, что в работе мы использовали токсин паука, открытый академиком Евгением Гришиным в 1986 году. Получается, что те вещества, которые паук использует для убийства жертвы, мы применяем для исследования основ функционирования нервной системы, они же помогут в создании новых лекарственных препаратов для лечения нейродегенеративных заболеваний», —добавляет Александр Василевский, преподаватель МФТИ и заведующий лабораторией в Институте биоорганической химии им. академиков М. М. Шемякина и Ю. А. Овчинникова РАН.
Здесь важно отметить, что токсины и их синтетические аналоги блокируют селективно те рецепторы, которые хорошо пропускают кальций. Они не влияют на непроницаемые для кальция рецепторы, наиболее важные для проведения нервных импульсов в мозге. Преимущество препаратов, которые будут синтезированы по образу и подобию токсинов, — в том, что они заблокируют только «патологические» рецепторы и не тронут физиологически важные.
Теперь, когда известно, как токсины и их синтетические аналоги связываются в канале глутаматного рецептора, химики смогут спроектировать новые, более эффективные блокаторы. Они будут препятствовать прониканию в принимающие нейроны излишнего кальция во время заболеваний нервной системы. Это спасет нервные клетки от гибели и восстановит нормальное функционирование нервной системы.